不睡覺為什么會死?Nature論文揭示,答案在于線粒體
https://news.cnblogs.com/n/799630/
來源 | 生物世界
撰文丨王聰
編輯丨王多魚
排版丨水成文
在生命進化的浩瀚畫卷中,鮮有生物創新能像有氧呼吸那樣深刻地改變生命存在的軌跡。有氧呼吸在數十億年前出現,利用了富含能量的氧氣,進而引發了一系列復雜性的連鎖反應,最終導致多細胞生物的崛起。這一進化里程碑與地球大氣中氧氣含量的重大變化緊密相關。通過優化細胞內電子轉移過程的效率,有氧呼吸釋放出了前所未有的能量產出,這些生化進步為寒武紀大爆發奠定了基礎,這一關鍵事件見證了生命形式的驚人多樣化,復雜的神經系統也在這時期出現。
神經系統對于快速的信息處理和生存行為至關重要,但其對能量的需求極大,給生物體帶來了巨大的代謝負擔。但有趣的是,這種代謝負擔似乎推動了睡眠行為的進化。然而,我們為何必須要睡眠?睡眠行為的生物學起源是什么?直到現在依然是未解之謎。
睡眠是一種在所有動物物種中都得以保留的不可或缺的行為,長期睡眠剝奪會導致死亡。之前的研究認為,睡眠發揮著神經元突觸維護以及記憶鞏固等功能,但越來越多的證據表明,睡眠的背后有著一個古老的代謝需求。
近日,牛津大學的研究人員在國際頂尖學術期刊 Nature 上發表了題為:Mitochondrial origins of the pressure to sleep 的研究論文。
該研究發現,睡眠壓力源自特定腦細胞中線粒體的 ATP 過剩,表明了睡眠或許不只是大腦的休憩,還可能是身體能量供應系統必不可少的維護過程。這一發現為生物體的睡眠驅動力提供了物理層面的解釋,并可能重塑我們對睡眠、衰老以及神經系統疾病的認知。

為了全面、無偏倚地探究大腦中可能驅動睡眠需求的分子機制,研究團隊對果蠅(常用的睡眠模式動物)進行了研究,對比分析了睡眠充足與睡眠剝奪的果蠅的單細胞轉錄組特征。
研究發現,在睡眠剝奪后,僅特定投射至中央復合體背扇形體(dorsal fan-shaped body,dFBN)的睡眠調控神經元(而非全腦范圍)中出現顯著上調的基因轉錄和表達,而且,這些上調的基因幾乎清一色是編碼與線粒體呼吸鏈功能和 ATP 合成相關的蛋白質。這強烈暗示了睡眠不足對這些神經元的能量代謝系統產生了巨大沖擊。
研究團隊進一步觀察了這些受影響的神經元內的線粒體變化——線粒體“碎片化”。具體來說,這些基因表達上調變化伴隨著線粒體分裂加劇、線粒體自噬增強,以及線粒體-內質網膜接觸位點的增加。此外,線粒體的這些形態學改變可通過恢復睡眠來逆轉,而在呼吸鏈中引入電子泄漏系統則能抑制該現象。
人工干預 dFBN 神經元的線粒體分裂/融合過程會雙向調控睡眠:誘導線粒體過度融合可提升神經元興奮性,增加睡眠時長,而促進線粒體分裂,則降低神經元興奮性,減少睡眠時長。
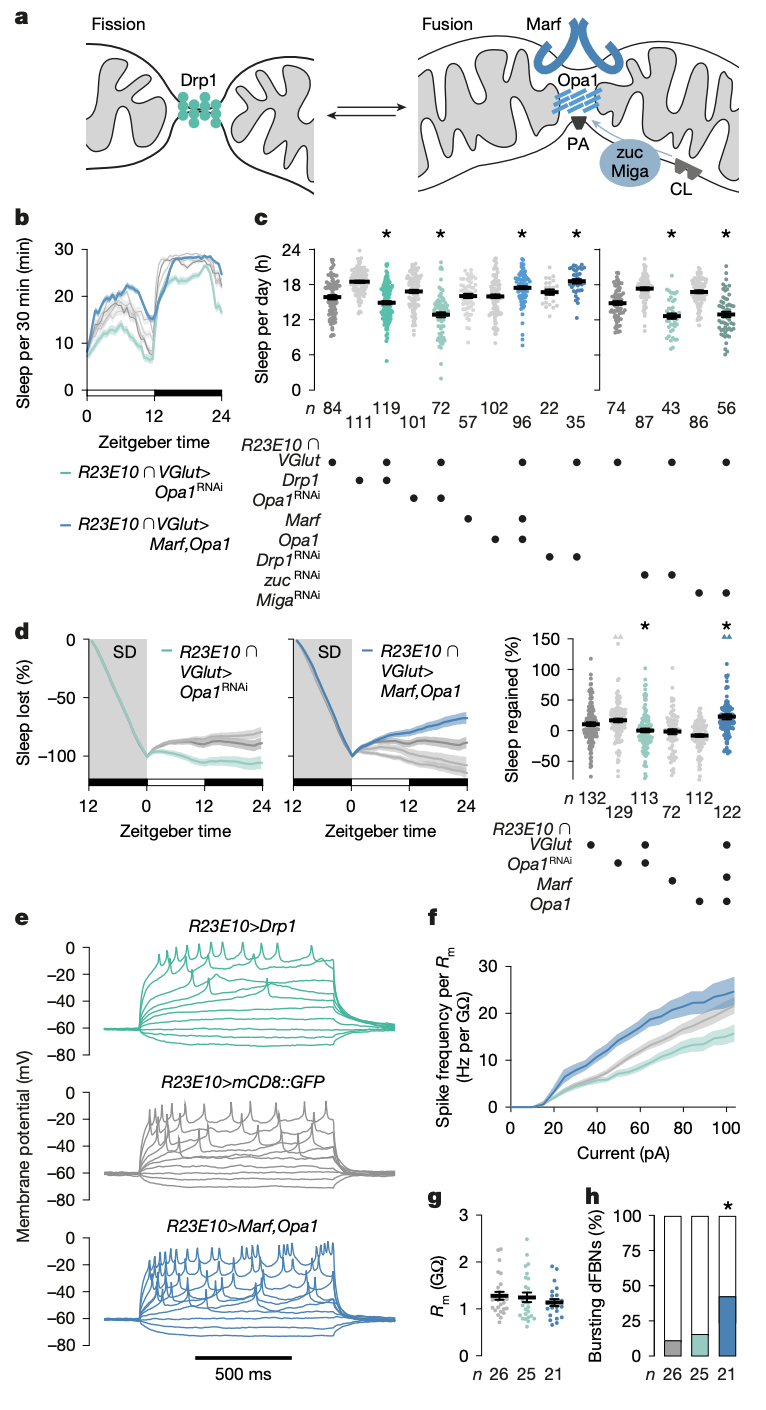
線粒體動力學改變睡眠
那么,為什么線粒體的分裂或融合會影響 dFBN 神經元的活動,進而影響睡眠需求呢?
研究團隊發現,清醒時(尤其是通過睡眠剝奪而強制清醒),dFBN 神經元活動被抑制,以減少睡眠沖動,但它們仍在繼續攝入能量物質,但因為神經元活動低,ATP 消耗減少,線粒體電子漏增加,最終造成神經元內 ATP 濃度反而升高。線粒體碎片化(線粒體分裂增加)、線粒體-內質網接觸點增加(利于受損脂質修復)和線粒體自噬增強(清除受損線粒體),都是為了應對這種 ATP 過剩以及潛在的氧化壓力的反應。也就是說,線粒體的分裂降低了 dFBN 神經元興奮性,使其難以啟動促睡眠,而線粒體的融合增加了 dFBN 神經元興奮性,使其啟動促睡眠。
研究團隊進一步驗證,人為解偶聯電子傳遞鏈與 ATP 合成,讓電子傳遞不完全用于 ATP 合成,能夠降低睡眠需求;而通過光控質子泵不依賴電子傳遞直接合成 ATP ,則增加了睡眠需求。這些結果表明,睡眠或許與衰老類似,是需氧代謝過程中無法避免的生理代償機制。
這些發現也有助于解釋新陳代謝、睡眠和壽命之間眾所周知的關聯——體型較小的動物每克體重消耗的氧氣更多,因此它們往往睡眠時間更長,壽命更短;患有線粒體疾病的人,即使不運動也常常會感到極度疲勞和困倦。
這項研究的意義非凡,首次定位了睡眠壓力的核心——投射至中央復合體背扇形體的睡眠調控神經元(dFBN 神經元);解析了線粒體形態動力學(分裂、融合)是調控神經元興奮性和睡眠需求的關鍵開關,其背后是線粒體的電子供給和 ATP 需求的匹配問題;揭示了睡眠壓力的本質——和衰老一樣,可能是需氧代謝帶來的一個不可避免的副產物,高效的能量生產需要付出額外維護成本,睡眠可能是關鍵的維護期;為理解失眠、嗜睡以及輪班工作的健康影響提供了全新的細胞和分子視角,未來或可通過調控特定神經元的線粒體功能和形態來干預睡眠障礙。這些發現也再次證明了線粒體在生物學中的核心地位——它們不僅是能量工廠,更是關鍵的信息處理器和生命最基本節律(睡眠節律)的調節器。
論文鏈接:
https://www.nature.com/articles/s41586-025-09261-y



 浙公網安備 33010602011771號
浙公網安備 33010602011771號